遺伝性ATTRアミロイドーシスの治療の現状と今後の展望
Pharma Medica 37(1):71-74, 2019
遺伝性ATTRアミロイドーシスとは
“遺伝性ATTRアミロイドーシス” とはどのような疾患なのでしょうか?
遺伝的に変異した異型トランスサイレチン(TTR)を原因タンパク質とする遺伝性疾患です。TTRは通常4量体で機能しますが,異型TTRが存在するとこの構造が不安定になり,単量体となって体内を循環するようになります。すると,TTRがミスフォールディングを起こしてアミロイド化し,それが末梢神経や心臓,腎臓などに沈着して,全身臓器にさまざまな障害をもたらします(図1)。疾患特異的な症状はありませんが,下肢の感覚障害などのポリニューロパチーを呈するほか,自律神経障害として,下痢や便秘,嘔吐などの消化器症状が認められることがあります。そのほか,図1のような多彩な症状がみられます。
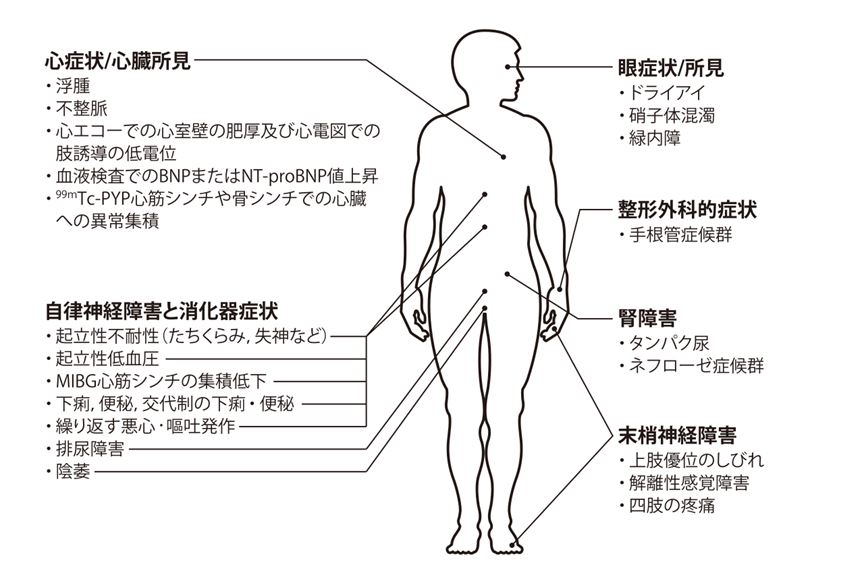
図1 遺伝性ATTRアミロイドーシスの臨床症状
(安東先生ご提供)
日本にはどのくらいの患者さんがいるのでしょうか?
私たちが行った疫学調査研究から,確定診断に至っておらず未治療の方も含めると,1,000人以上の患者さんがいると推定しています。本邦では主に熊本県と長野県に集積地があると考えられていましたが,近年,遺伝歴がはっきりしない,集積地とは異なる遺伝子変異を有する孤発型の遺伝性ATTRアミロイドーシスが全国各地で明らかにされてきています。このような孤発型の遺伝性ATTRアミロイドーシスは,50歳以上で発症することが多く,超高齢社会で平均寿命が延びたことから顕在化してきたと考えられます。遺伝性ATTRアミロイドーシスは,希少疾患であることに加え,特異的な臨床症状がなく,全身に多彩な症状を呈することから,診断が難しく,確定診断までに時間を要するケースが多いのが現状です。多くの方が適切な治療がなされないまま,病勢が進行している可能性があります。
このような状況の中,熊本大学神経内科では,熊本県の地域医療再生計画より補助を受けて,「アミロイドーシス診療体制構築事業」に取り組み(図2),一人でも多くの患者さんを発見して,少しでも早く適切な治療を受けていただけることを目的に,アミロイドーシス診療センターを開設しました。国内外から年間500例以上の診断依頼を受け,毎年50~60例が遺伝性ATTRアミロイドーシスと診断されており,顕在化する患者数は年々増加しています。原因不明のポリニューロパチーや全身症状を呈する患者さんに出会った場合は,ATTRアミロイドーシスの可能性を疑って,当センターへご相談いただければと思います。
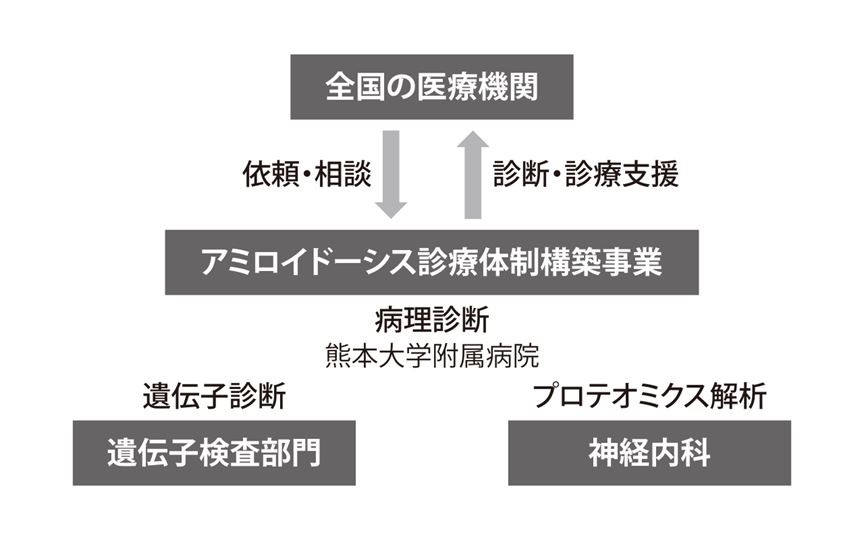
図2 アミロイドーシス診療体制構築事業の概要
(安東先生ご提供)
遺伝性ATTRアミロイドーシスの治療
現在の治療法について教えてください。
TTRの95%以上が肝臓で産生されるため,遺伝性ATTRアミロイドーシスを根治させる治療としては現時点では肝移植しかありません。60歳未満,発症後5年未満で日常の活動を行う能力がある,重篤な心・腎機能障害がないなどの条件を満たした患者さんが肝移植の対象となり,術後の症状進行がほとんど停止するだけでなく,生命予後も改善することが明らかになっています1)。ただし,移植後も網膜の色素上皮細胞から異型TTRが産生されるため,アミロイド沈着による眼症状は移植によっては阻止できないこと2),移植後も心症状や心肥大が進行することなども示されています3)。また,ドナー不足も大きな課題といえます。
肝臓移植以外の治療法はありますか?
本邦で承認されている薬剤としてタファミジスがあります。タファミジスは経口剤であり,TTRの4量体構造を安定化させる作用があります。発症後早期に服用を開始すればアミロイドーシスにおける神経障害の進行を抑制してQOLの維持が期待できます4,5)。異型TTRは産生され続けるので完治は望めませんが,肝移植に適合しない高齢の患者さんや肝移植を待つ患者さんなどに投与されています(図3)6)。
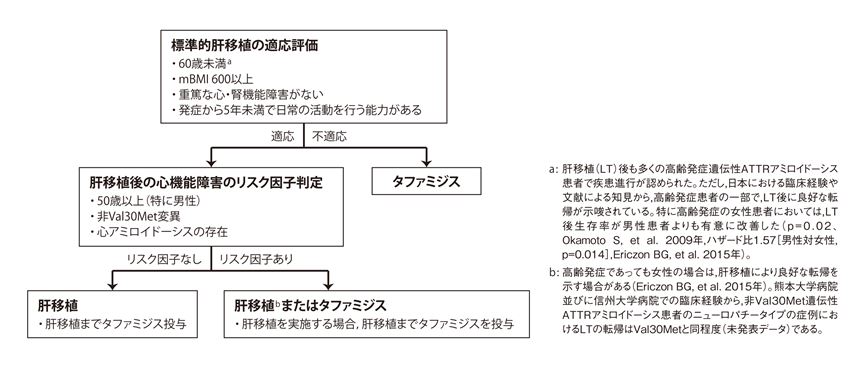
図3 日本における遺伝性ATTRアミロイドーシスの治療アルゴリズム
(Sekijima Y, et al: Orphanet J Rare Dis 13(1) : 6, 2018)
また,タファミジスに関しては,2018年8月に,TTR型心アミロイドーシスを対象とした国際共同第Ⅲ相試験(ATTR-ACT試験)の成績が発表されました7)。全死因死亡率と心血管関連入院の頻度が,プラセボ群に比べて,タファミジス群で有意に低下したという結果です。この試験には,遺伝性ATTRを有する患者さんだけでなく,老化に伴って起こり得る野生型ATTRを有する患者さんも登録されていました。
一方,それとほぼ同時期に,TTR自体の産生を抑える薬剤としてsiRNA(small interfering RNA)による核酸医薬が欧米で承認され,本邦でも間もなく臨床導入されようとしています。
siRNAによる治療について詳しく教えてください。
siRNAは,mRNAを標的とした遺伝子サイレンシング治療(gene silencing)の一つで,特定の遺伝子の働きを眠らせることで疾患の治癒を目指すという,これまでにはなかった全く新しい作用機序を有する次世代の新薬として注目されています。
欧米で承認されたパチシランは,TTRのmRNAの分解を促すことで肝臓でのTTR産生を特異的に阻害する世界初のsiRNA製剤です。ポリニューロパチーを伴う遺伝性ATTRアミロイドーシス患者を対象に行われた国際共同第Ⅲ相試験(APOLLO試験)において,パチシラン(0.3mg/kg体重)を3週ごとに静脈内投与する群とプラセボを投与する群で,それぞれの有効性と安全性が比較検討されました8)。その結果,投与開始18ヵ月時点の修正ニューロパチー障害スコア(mNIS+ 7)やQOLスコア(Norfolk QOL-DN)は,プラセボ群に比べて,パチシラン群で有意に改善することが示されました。また,血清中TTR濃度は,年齢や性別,TTRの変異型にかかわらず約81%低下しました。さらに,心病変を有する患者集団を対象としたサブグループ解析によって,パチシラン群で心臓の機能だけでなく構造も有意に改善することが確認されました8,9)。なお,プラセボ群と比較して,パチシラン群において特に臨床的に問題となる副作用は認められていません。
遺伝性ATTRアミロイドーシスの根本的な治療はこれまで肝移植しかありませんでした。しかし,パチシランが登場したことで内科的に根治を目指せる時代が到来したといえるでしょう。現在,パチシランの改良型製剤としてALN-TTRsc02も開発されています。ALN-TTRsc02は,年4回程度の皮下注射で,遺伝性だけでなく野生型のATTRアミロイドーシスに対する臨床効果が検討されていますので,より多くの患者さんにそのメリットが享受されることを期待しています。
ATTRアミロイドーシスの診療における課題と今後の展望
ATTRアミロイドーシスの診療における課題点を教えてください。
ATTRアミロイドーシスには,これまでお話ししてきた遺伝性ATTRアミロイドーシスのほかに,遺伝子の異常ではなく,老化によって生じた異型TTRの沈着が原因で発症する野生型ATTRアミロイドーシス(別名:老人性全身性アミロイドーシス)があります。人類は進化の過程で,感染症や血液凝固異常などに対する防御系は獲得してきましたが,これほど寿命が延びることは想定されておらず,加齢によって起こり得るタンパク質の変性(アミロイドーシス)に対する防御系はまだ備わっていません。野生型ATTRアミロイドーシスは,老年期アルツハイマー型認知症と同様に,人類の寿命が延びたことで顕在化してきた,超高齢社会が生み出した新たな疾患といっても過言ではありません。
野生型ATTRアミロイドーシスの患者さんも多くが潜在化しているのでしょうか?
スウェーデンの調査では,80歳以上の剖検において25%に心臓へのアミロイド沈着(心アミロイドーシス)が観察されたことが報告されています10)。また,私たちの調査でも,80歳以上の15%に心アミロイドーシスを確認しています。総務省統計局による調査(平成30年9月1日現在)では,80歳以上の人口は1,104万人と推計されているので11),単純計算すると約160万人以上が心アミロイドーシスに罹患している可能性が示唆されます。
今後はどのような対策が必要だとお考えですか?
野生型ATTRアミロイドーシスはこれまであまり注目されてきませんでした。しかし,超高齢社会を迎えた今,見逃してはならない日常診療に潜む重大な疾患の一つとして認識する必要があります。加齢に伴う生体現象によって発症する代表的な疾患として,動脈硬化などの血管疾患やDNA変異による悪性腫瘍があります。これらの疾患については,広く認知されていますが,タンパク質のアミロイド化が原因で発症するアミロイドーシスについては,十分に認知されていない上,診断や診療の体制も十分整っていないのが現状です。今後は,遺伝性,野生型を問ず,ATTRアミロイドーシスの疾患重要性を広く啓発し,早期診断・早期治療が行える診療体制を構築していくことが重要だと考えます。
最後に今後の展望について,お聞かせください。
遺伝性ATTRアミロイドーシスの根本的な治療はこれまで外科的な肝移植しかありませんでした。しかし,siRNA製剤が登場したことで,今後は患者さんにとって侵襲的な負担が少ない内科的治療で根治が目指せる時代になっていきます。ただし,ATTRアミロイドーシスの多くの患者さんはさまざまな臓器にアミロイドがすでに沈着していることから,新薬を投与してもすぐに症状が改善するわけではありません。私たちは,すでに沈着しているアミロイドを標的とした抗体治療も開発中です(図4)。この抗体治療とタファミジスやsiRNAを併用すれば,沈着しているアミロイドを減らすと同時に,アミロイドの供給源を阻止することができ,より効果的な治療が行えると考えています。今後も,遺伝性をはじめ野生型も含めたATTRアミロイドーシスの患者さんを一人でも多く救えるよう,診療体制の構築を進めるとともに,病態解明と新たな治療に向けた研究に取り組んでいきたいと思います。
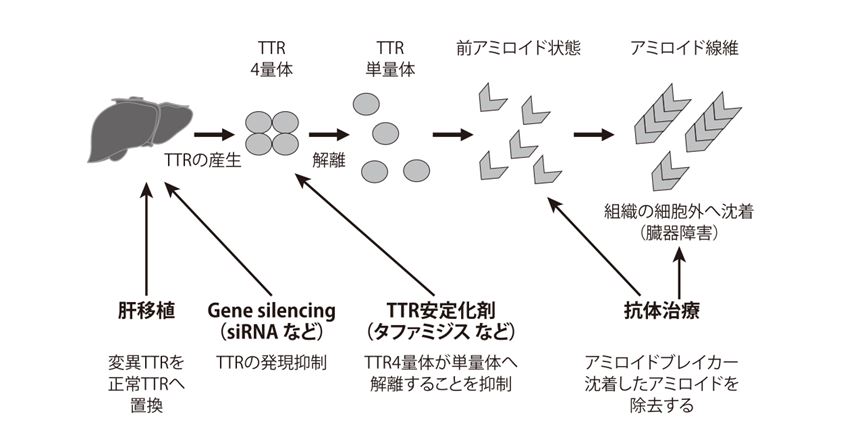
図4 ATTRアミロイドーシスの病態と治療標的
(安東先生ご提供)
- Yamashita T, Ando Y, Okamoto S, et al: Long-term survival after liver transplantation in patients with familial amyloid polyneuropathy. Neurology 78(9) : 637-643, 2012
- Ando Y, Ando E, Tanaka Y, et al: De novo amyloid synthesis in ocular tissue in familial amyloidotic polyneuropathy after liver transplantation. Transplantation 62(7) : 1037-1038, 1996
- Oshima T, Kawahara S, Ueda M, et al.: Changes in pathological and biochemical findings of systemic tissue sites in familial amyloid polyneuropathy more than 10 years after liver transplantation. J Neurol Neurosurg Psychiatry 85(7) : 740-746, 2014
- Coelho T, Maia LF, Martins da Silva A, et al: Tafamidis for transthyretin familial amyloid polyneuropathy: a randomized, controlled trial. Neurology 79(8) : 785-792, 2012
- Ando Y, Sekijima Y, Obayashi K, et al: Effects of tafamidis treatment on transthyretin (TTR) stabilization, efficacy, and safety in Japanese patients with familial amyloid polyneuropathy (TTR-FAP) with Val30Met and non-Val30Met: A phase III, open-label study. J Neurol Sci 362: 266-271, 2016
- Sekijima Y, Ueda M, Koike H, et al: Diagnosis and management of transthyretin familial amyloid polyneuropathy in Japan: red-flag symptom clusters and treatment algorithm. Orphanet J Rare Dis 13(1) : 6, 2018
- Maurer MS, Schwartz JH, Gundapaneni B, et al: Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med 379(11) : 1007-1016, 2018
- Adams D, Gonzalez-Duarte A, O'Riordan WD, et al: Patisiran, an RNAi therapeutic, for hereditary transthyretin amyloidosis. N Engl J Med 379(1) : 11-21, 2018
- Solomon SD, Adams D, Kristen A, et al.: Effects of patisiran, an RNA interference therapeutic, on cardiac parameters in patients with hereditary transthyretin-mediated amyloidosis: An analysis of the APOLLO study. Circulation. doi:10.1161/CIRCULATIONAHA. 118.035831
- Westermark P, Bergström J, Solomon A, et al.: Transthyretin-derived senile systemic amyloidosis: clinicopathologic and structural considerations. Amyloid 10(Suppl 1) : 48-54, 2003
- 総務省統計局:人口推計(平成30年9月1日現在概算値)

